La suite logicielle Ennov Clinical
Aux États-Unis, on estime le coût associé à la conduite d’essais cliniques à 20 millions de dollars pour un essai de phase I, et jusqu’à 100 millions de dollars pour un essai de phase III. Chaque année, les promoteurs d’essais cliniques investissent des millions de dollars dans l’espoir d’améliorer l’efficacité des essais et d’en diminuer les coûts grâce à la technologie.
La suite de logiciels Ennov Clinical fournit aux promoteurs, aux CRO, aux investigateurs et aux patients une solution complète de bout-en-bout pour la capture et la gestion de toutes les informations, structurées ou non, associées aux essais cliniques, des premières étapes de leur planification, jusqu’à leur exécution et leur finalisation. La suite Ennov Clinical comprend des applications de data management pour essais cliniques (Ennov EDC, Ennov RTSM et Ennov ePRO) et des applications de gestion des essais cliniques (Ennov CTMS et Ennov eTMF), qui peuvent être déployées dans le cloud ou sur site. Notre application Ennov Clinical eLearning vient compléter cette suite logicielle innovante.
Avantages
- Unique source de vérité : Gérez et suivez l’ensemble des données, la documentation et les processus cliniques dans une unique solution pour rationaliser les opérations cliniques et gagner en efficacité.
- Meilleures performances : Éliminez le papier et la saisie manuelle de vos processus. Automatisez les tâches répétitives et sources d’erreur pour de formidables gains de productivité.
- Connectivité globale : Encouragez la collaboration au-delà des départements et des frontières géographiques grâce à une solution commune unifiée disposant d’une interface utilisateur intuitive et localisable.
- Meilleure visibilité : Obtenez des informations précieuses sur vos essais cliniques afin d’identifier et prévenir les tendances problématiques avant qu’elles ne conduisent à des problèmes qualité.
EDC
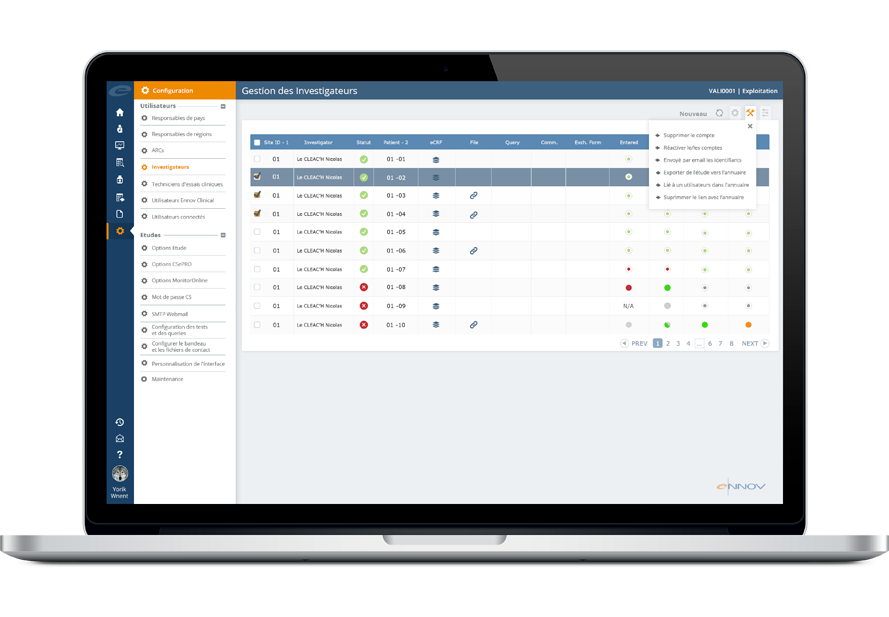
Logiciel eCRF efficace et conforme
Avec Ennov EDC, créez une étude EDC et collectez facilement des données cliniques : fini les problèmes de conformité, de traçabilité, de données manquantes ou erronées ! Ennov EDC est une solution complète unique, qui permet aux gestionnaires de données de concevoir, déployer et capturer des données cliniques multicentriques. Les essais cliniques de toute taille sont supportés, y compris les essais cliniques internationaux complexes. Grâce à Ennov EDC, capturez des données plus complètes et plus exactes, tout en améliorant la communication entre les équipes cliniques. Son intégration native avec Ennov ePRO permet également aux patients d’enregistrer leur autojournal et leur questionnaire qualité de vie. Avec Ennov EDC, rationalisez significativement la randomisation, le design des essais, les tests de cohérence, le codage médical (MedDRA, WHO Drug), et l’import / export des données.
RTSM
Rationalisez la randomisation et la gestion des approvisionnements avec Ennov RTSM
Ennov Clinical incorpore un système de randomisation directe des patients au sein de son logiciel eCRF. Notre solution IWRS (Interactive Web Response Service) propose de nombreuses options, telles que le contrôle de l’éligibilité par des prétests de cohérence, le choix des strates et de la méthode de randomisation (blocs, minimisation), l’activation du “facteur de randomisation” et la gestion de l’approvisionnement en produits candidats. Notre logiciel facilite la gestion d’une étude en double aveugle et prévient toute anticipation d’allocations ultérieures. Le module Ennov Randomization vous permet d’obtenir une vision globale de la randomisation de tous les patients (c.-à-d. le succès ou l’échec) ou du patient individuel (diverses opérations de randomisation ou d’allocations de médicaments).
ePRO
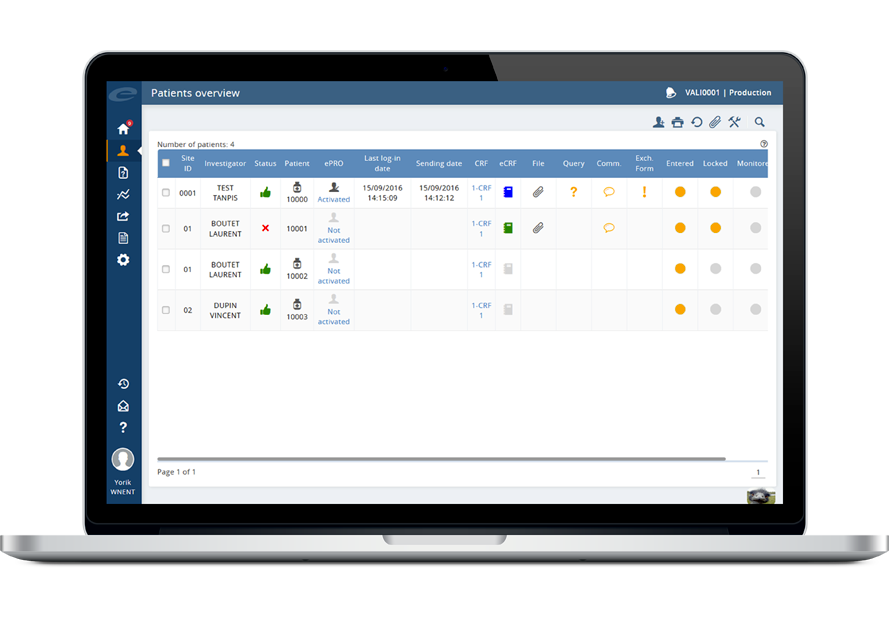
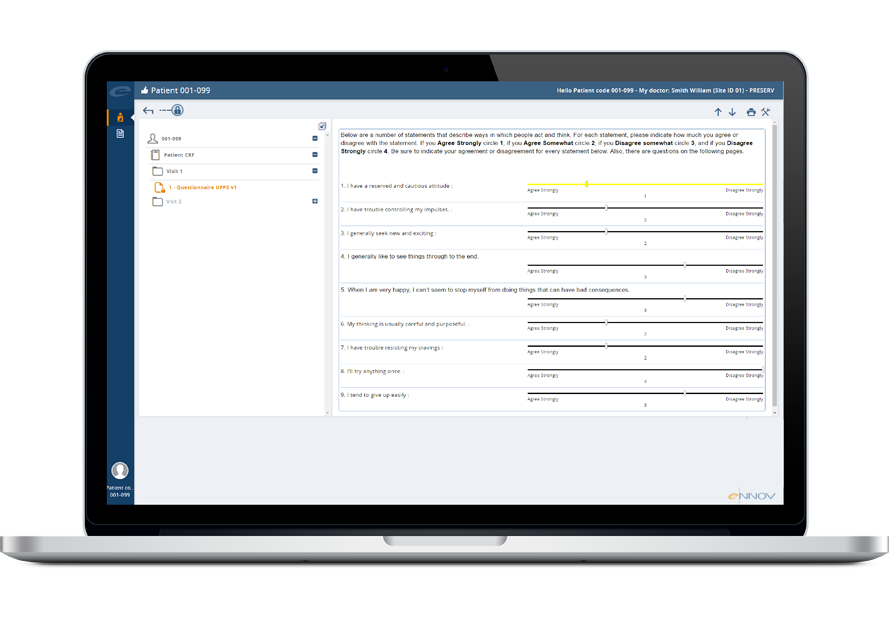
Avec le logiciel Ennov ePRO, capturez facilement les données électroniques des patients
Lors d’essais cliniques, l’évaluation de l’efficacité d’un médicament et de la qualité de vie des participants repose notamment sur les données autodéclarées par ces derniers. Toutefois, l’utilisation de questionnaires papier s’avère souvent fastidieuse et complexe à gérer, en particulier dans le cas d’essais cliniques internationaux complexes, où il peut être délicat de s’assurer de la collaboration et de l’observance des participants.
Avec Ennov ePro, automatisez la capture des données électroniques des participants ! L’utilisation de questionnaires en ligne permet non seulement aux patients de répondre en toute confidentialité depuis le confort de leur domicile, mais également de mettre immédiatement à disposition des investigateurs et des promoteurs des essais cliniques les données renseignées. En outre, ces questionnaires se construisent grâce au même outil de conception simple et intuitif utilisé par Ennov EDC !
CTMS
Monitorez efficacement vos essais cliniques du début à la fin grâce au logiciel complet de gestion des essais cliniques d'Ennov
Chaque année, les promoteurs d’essais cliniques recherchent de nouvelles méthodes pour en améliorer l’efficacité et en diminuer les coûts. Plusieurs actions vont permettre d’améliorer l’efficacité opérationnelle et la productivité du site investigateur : la centralisation des informations, une surveillance active de la progression, l’automatisation de la programmation des visites, la gestion financière, ainsi qu’un reporting et des indicateurs précis. Ennov CTMS permet aux promoteurs et CRO d’adresser activement, depuis une plateforme unique, tous les aspects de la gestion d’essais cliniques : sites investigateurs, patients, événements indésirables, écarts, inclusions, rapports de visite, contacts téléphoniques, gestion des médicaments expérimentaux, centres investigateurs et aspects financiers.
Le tableau de bord CTMS fournit aux chef de projet des analyses à la demande, permettant ainsi d’améliorer la qualité, de contrôler les risques et de réduire les coûts. Désormais en mesure de planifier et suivre leurs essais en temps réel, les chefs de projet prennent de meilleures décisions, plus rapidement.
eTMF
Prenez votre documentation clinique en main et soyez toujours prêts en cas d'inspection
La documentation, essentielle pour les essais cliniques, est indiscutablement l’une des activités les plus prenantes et les plus coûteuses associées à leur conduite. Le texte des bonnes pratiques cliniques ICH E6 spécifie une liste de plus de 200 documents distincts devant être gérés avant, pendant et après l’essai clinique. L’ensemble, ou chacun, de ces documents doit être disponible pour audit par le promoteur et inspection par les autorités réglementaires. Étant donné le volume important de documentation associé au processus, une gestion documentaire efficace pourra avoir un impact significatif sur les coûts et les délais nécessaires à la finalisation de l’essai clinique.
Ennov eTMF met la puissance d’Ennov Doc, notre GED complète et facile à utiliser, au service de nos clients : prenez en main votre documentation réglementaire et soyez toujours prêts en cas d’inspection !
TMF Archive
Découvrez la sérénité d'avoir une archive TMF sûre et inspectable
Même si vos TMF (Trial Master Files) ne sont pas gérés sur site, il est possible que vous ayez besoin d’archiver les TMF fournis par vos partenaires. Ou peut-être recherchez-vous une alternative vous permettant d’éviter les frais élevés demandés par votre fournisseur pour l’archivage de TMFs de votre eTMF actif ?
Avec Ennov eTMF Archive, bénéficiez d’un répertoire sûr et économique, facile à naviguer et conforme à toutes les réglementations ! Grâce à une interface utilisateur intuitive et à un référentiel de documents respectant le “TMF Reference Model” du DIA, les inspecteurs trouveront rapidement les documents nécessaires à la reconstruction de votre essai. De plus, la focalisation sur les fonctionnalités d’archivage en lecture seule permet de réduire fortement les coût et durées de formation.